A toxoplasmose é a uveíte posterior mais comum no Brasil. Sendo assim, é algo que faz parte da nossa rotina desde o início da residência médica. Com esse conteúdo, nosso objetivo é principalmente servir de consulta prática para revisão e especialmente para a prescrição do tratamento.
DEFINIÇÃO
Assuntos abordados
Vamos relembrar brevemente o ciclo do parasito causador da Toxoplasmose, o que nos ajuda a entender e também a explicar aos pacientes sobre as formas de contágio e evolução clínica. O hospedeiro suscetível se contamina ao ingerir oocistos maduros ou ao entrar em contato com taquizoítos (eliminados na urina, leite, esperma e perdigotos) ou ao ingerir carne crua ou mal cozida contendo taquizoítos ou cistos com bradizoítos. Os parasitas que sobrevivem ao suco gástrico penetram no sangue e irão se espalhar e reproduzir nas mais diversas células do organismo (fase aguda). Após o controle imunológico, permanecem em fase cística tecidual (fase crônica), podendo haver recidivas a depender do estado imunológico.
QUADRO CLÍNICO
- Crianças com toxoplasmose ocular podem se apresentar com queixa de baixa visão, estrabismo, nistagmo ou leucocoria.
- Adultos podem se apresentar com queixa de baixa visão, moscas volantes, dor ocular, fotofobia e hiperemia conjuntival.
- 2/3 dos pacientes com toxoplasmose ocular podem apresentar recorrência.
EXAME FÍSICO DA TOXOPLASMOSE OCULAR
Forma típica: Retinocoroidite
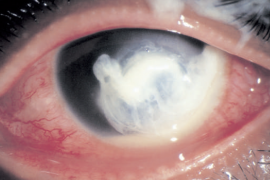
A toxoplasmose ocular pode se apresentar mais classicamente como lesão retiniana exsudativa, única ou múltipla (retinocoroidite granulomatosa focal necrosante). O aspecto de “farol na neblina” é típico (figura 1). No segmento anterior pode haver reação de câmara anterior, precipitados ceráticos (incluindo mutton-fat), nódulos irianos e sinéquias posteriores. O quadro é auto limitado (6-8 semanas).
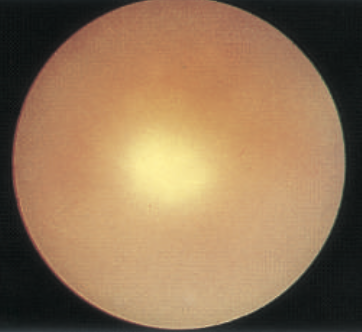
Fonte: BCSC 2020-2021: Uveitis and ocular inflammation, p. 278.
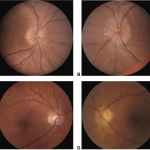
Após a resolução do quadro ativo da toxoplasmose, forma-se uma cicatriz, de margens bem delimitadas, com vários graus de hiperplasia do epitélio pigmentado da retina e com atrofia retinocoroideana. A cicatrização ocorre da periferia para o centro.
A presença de uma lesão satélite (figura 2) sugere fortemente o diagnóstico de toxoplasmose ocular (proximidade de uma lesão cicatrizada próxima à ativa).

Fonte: BCSC 2020-2021: Uveitis and ocular inflammation, p. 278.
Existem outras formas de apresentação da toxoplasmose ocular adquirida, que são ditas atípicas.
Elas incluem: retinite punctata externa; neurorretinite; neurite; forma pseudomúltipla ou ainda reações inflamatórias intraoculares sem lesão focal posterior necrosante em pacientes com toxoplasmose adquirida sistêmica.
Puntata externa
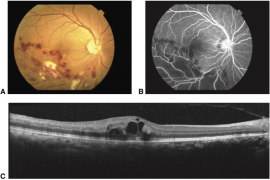
- Pequenas lesões branco-acinzentadas, multifocais, ao nível da retina externa e EPR (figura 3).
- Caráter recorrente
- Vitreíte leve
- Acometimento grave do nervo óptico, com palidez intensa
- Ocorre geralmente nas primeiras e segunda décadas de vida
- Congênita ou adquirida
- Bilateral em 1/3 dos casos
- Diagnóstico diferencial de neurorretinite subaguda unilateral difusa (DUSN)

Fonte: Série Oftalmologia Brasileira, Uveítes, 3 ed, p. 155.
Neurorretinite por toxoplasmose
- Inicia-se como papilite isolada e após alguns dias evolui com foco de retinocoroidite justadiscal
- Diagnóstico diferencial com a doença da arranhadura do gato.
COMPLICAÇÕES DA TOXOPLASMOSE OCULAR
- Glaucoma
- Catarata
- Vitreíte crônica
- Hemorragias vítreas por avulsão de vasos causada pela retração do vítreo
- Hemorragias retinianas por oclusão de veias adjacentes à lesões em atividade
- Atrofia óptica
- Edema macular cistoide
- Buraco macular
- Membrana epirretiniana
- Phthisis bulbi
DIAGNÓSTICO
- Os testes sorológicos são úteis para auxiliar no diagnóstico de toxoplasmose ocular, já que o resultado negativo pode descartar a hipótese, mas o positivo não confirma o diagnóstico pela alta prevalência dos anticorpos na população. IgG fica positivo após 2 semanas da infecção e geralmente se mantém positivo durante toda a vida. Já o IgM pode permanecer detectável até 1 ano após a infecção.
- Angiofluoresceinografia, OCT e ecografia podem ser úteis em casos de toxoplasmose ocular com complicações.
TRATAMENTO
Segundo a Sociedade Brasileira de Uveítes, os critérios para tratamento da toxoplasmose ocular adquirida são:
- Ameaça de áreas nobres (mácula, região perimacular, disco óptico e região peridiscal)
- Vitreíte intensa
- Inflamação intensa
- Lesões crônicas e exsudativas extensas, independente da localização
Apesar disso, é habitual o tratamento em todos os casos diagnosticados de toxoplasmose ocular. O tratamento tem o benefício de reduzir a duração da replicação do parasita, levando a uma cicatrização mais rápida, menor cicatriz, reduzir a frequência de recorrências e minimizar complicações.
O preconizado pelo CBO como primeira opção é o dito “tratamento clássico” da toxoplasmose, composto por: sulfadiazina + pirimetamina + ácido folínico + prednisona.
- Sulfadiazina 500 mg, 2 cp de 6/6h durante 35 dias. Crianças: 50 a 100 mg/kg/dia.
- Pirimetamina 25 mg. Iniciar com dose de ataque de 4 cp no primeiro dia, 3 cp no segundo dia, seguida por 2 cp/dia por 45 dias. Criança: 1 mg/kg/dia.
- Ácido folínico 15 mg, 1 cp por dia por 45 dias.
- Prednisona 20 mg. Iniciar junto com o tratamento específico com 0,5 mg/kg/dia, reduzindo 10 mg a cada 6 dias até finalizar 10 dias antes do término do tratamento específico.
Porém, diversos serviços no Brasil adotam o Bactrim F® (sulfametoxazol + trimetoprima) como escolha para o tratamento da toxoplasmose ocular, por diversos motivos: melhor adesão do paciente ao tratamento; menos efeitos colaterais, principalmente gastrointestinais; maior facilidade de encontrar a medicação para compra. Porém, segundo o CBO, ele se torna primeira escolha para profilaxia, e não para tratamento.
Sulfametoxazol + Trimetoprima 800/160 – 1 cp de 12/12h durante 30 a 40 dias.
Em caso de intolerância à sulfadiazina, utilizar em associação à pirimetamina a:
Clindamicina 300 mg 1 cp 6/6h por 30-40 dias. Obs.: risco de colite pseudomembranosa durante o tratamento ou mesmo após a suspensão do mesmo.
O esquema de tratamento para gestantes será diferente conforme o trimestre da gestação:
- 1º trimestre: espiramicina + sulfadiazina.
- 2º trimestre: espiramicina + sulfadiazina + pirimetamina + ácido folínico (após 14ª semana);
- 3º trimestre: espiramicina + pirimetamina + ácido folínico
Espiramicina 1,5 mUI 6/6h durante 30 a 40 dias.
A espiramicina pode ser utilizada em toda a gestação justamente por não atravessar a placenta e não provocar efeitos colaterais indesejáveis ao feto, sendo como propósito principal de impedir ou retardar a passagem do toxoplasma para o feto.
Tratamento profilático
Indicado em caso de lesões recidivantes de toxoplasmose ocular.
Bactrim F 1 cp por dia (segunda, quarta e sexta-feira) durante 1 ano.
EFEITOS ADVERSOS DOS MEDICAMENTOS
- Sulfadiazina: derivado de sulfa que apresenta semelhança estrutural e antagonismo competitivo ao ácido paraminobezoico (PABA), impedindo sua utilização pelo parasita causador da toxoplasmose ocular na síntese do ácido fólico, tendo efeito sinérgico à pirimetamina. A sulfa pode apresentar deposição urinária, resultando em cálculos renais, cólica renal e hematúria; raramente pode gerar anemia hemolítica aguda, principalmente em crianças; agranulocitose; anemia aplástica; reações de hipersensibilidade; síndrome de Stevens-Johnson; hepatite e hipotireoidismo. É contra-indicada no terceiro trimestre da gestação. Caso haja efeitos colaterais genitourinários, deve-se estimular a ingesta hídrica e alcalinizar a urina.
- Pirimetamina: interrompe o ciclo metabólico do parasita causador da toxoplasmose ocular por inibir a enzima diidrofolatorredutase, impedindo a conversão de ácido fólico em ácido folínico. Portanto, deve ser usado juntamente com ácido folínico para reposição do mesmo. Pode causar, náuseas, vômitos, dor abdominal, perda de peso e da gustação, reação alérgica e depressão da medula óssea (10% dos casos). Deve ser suspenso caso hajam algum problema hematológico e é contraindicado no primeiro trimestre da gestação e na lactação.
- Clindamicina: antibiótico da classe das lincosamidas, tendo efeito principalmente bacteriostático (pode ser bactericida em concentrações maiores) por inibir a síntese proteica ligando-se à sub-unidade 50s do ribossomo. Nos pacientes com toxoplasmose ocular, é uma droga alternativa, usada em associação à pirimetamina, em casos de intolerância à sulfadiazina. Pode causar diarreia, exantema e mais gravemente colite pseudomembranosa, que pode surgir durante ou semanas após o tratamento, podendo ser fatal. Em caso de colite, deve ser suspensa imediatamente, podendo ser substituída por vancomicina.
- Sulfametoxazol-trimetoprima: a sulfonamida age impedindo a incorporação do PABA no ácido fólico e a trimetoprina impede a redução do diidrofolato em tetraidrofolato. Como efeito colaterais temos: anemia megaloblástica, leucopenia e trombocitopenia em caso de deficiência de folato, síndrome de Stevens-Johnson, icterícia, cefaleia, náuseas, vômitos, estomatite e comprometimento renal. Pode ser utilizada como único antibiótico em esquema de tratamento associado a prednisona.
REFERÊNCIAS BIBLIOGRÁFICAS
Série Oftalmologia Brasileira, Uveítes, 3 ed.
BCSC 2020-2021: Uveitis and ocular inflammation.